
根据基因与肥胖分型的关系,运用科学方法找出每个人特异的“肥胖基因”,规划有效健康瘦身计划,让减肥不再徒劳。
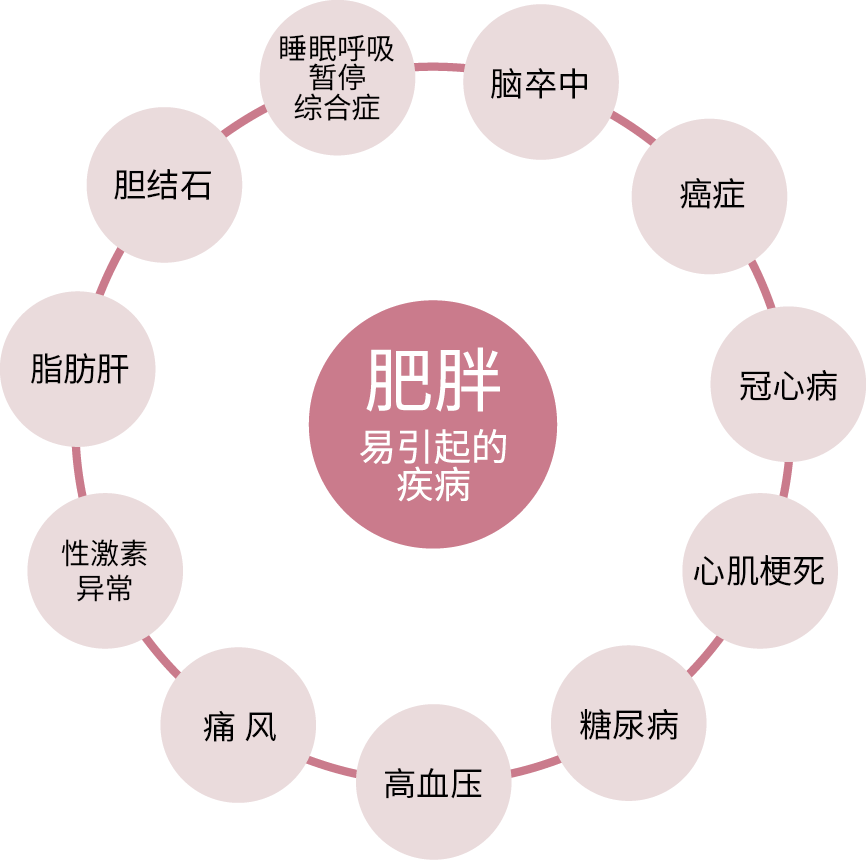
肥胖易引起的疾病
肥胖会引发很多的健康问题,如冠心病、高血压、糖尿病等,并且体脂含量越高,患病风险越大。脂肪代谢的异常可导致机体能量代谢障碍,从而导致肥胖的发生。因此,脂肪代谢在肥胖的发生、发展中起到关键的作用。
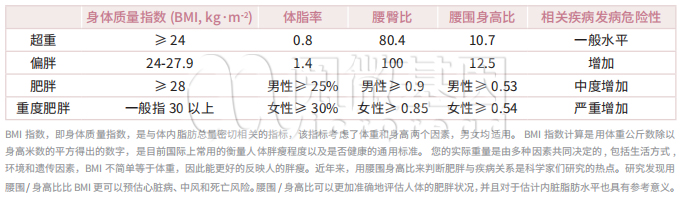
适用于中国的肥胖定义
检测内容
■ 减肥基因检测(2 项):脂肪代谢、运动减肥
适用人群
■ 非家族遗传性青少年肥胖者
■ 成年后肥胖或体脂率增高人群
■ 有健康 / 体重管理计划的人群
样本类型
■ 血样采集卡
■ EDTA/ 枸橼酸钠抗凝血
■ 口腔粘膜上皮细胞






